米バイオ医薬企業インテリア・セラピューティクスは27日、遺伝性血管性浮腫(HAE)に対する体内ゲノム編集治療薬の臨床試験で有効性を示す結果を得たと発表した。米食品医薬品局(FDA)への承認申請手続きを開始しており、承認されれば、ノーベル賞対象となったゲノム編集技術「クリスパー・キャス9」を体内で使用する世界初の治療法実用化となる見込みだ。2027年前半の発売を目標としている。
遺伝性血管性浮腫(HAE)とは
HAEは主に遺伝子変異が原因で、唇やまぶた、胃腸など様々な部位が繰り返し腫れる疾患。喉に症状が出ると呼吸困難を引き起こし、命に関わることもある。発症率は5万人に1人で、10代から20代で発症することが多い。既存の発作予防薬もあるが、効果が不十分な例も存在する。
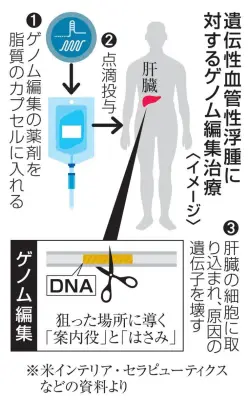
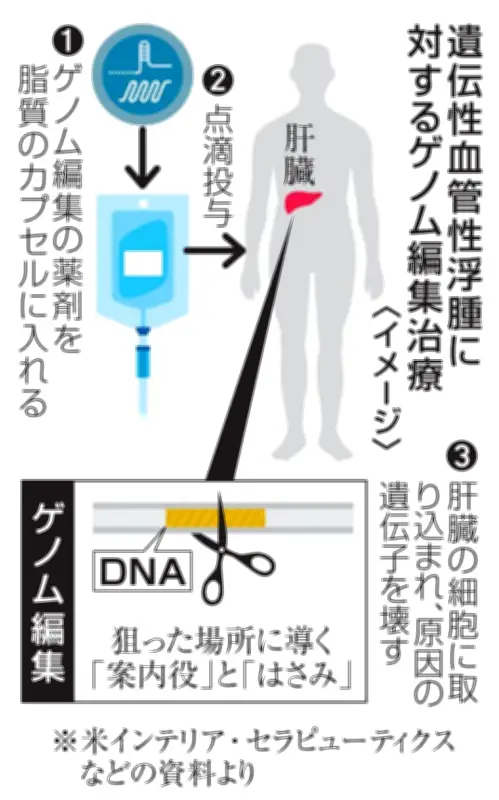
新治療薬の仕組み
新薬は、発作原因遺伝子を切断して機能を失わせる「ハサミ」役の酵素と、そのハサミを標的遺伝子に導く「案内役」分子で構成される。これらの成分を1回点滴投与すると、肝臓細胞に取り込まれ、原因遺伝子を破壊する。これにより、長期的な治療効果が期待される。
今回の臨床試験では、患者の症状発作頻度が有意に減少し、安全性も確認された。インテリア社は今後、FDAとの審査を経て、早期の承認を目指す。本治療の実用化は、遺伝性疾患に対する新たな治療の幕開けとなる可能性がある。